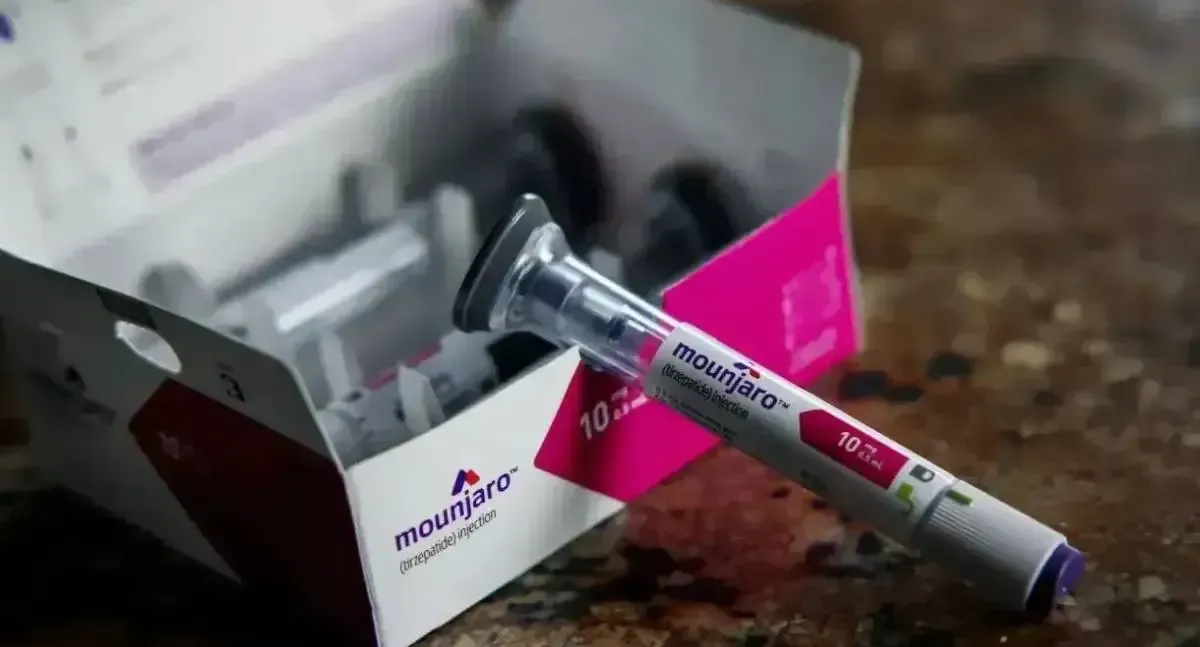
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, nesta quarta-feira (22), a ampliação do uso da tirzepatida, comercializada sob o nome Mounjaro, para o tratamento de diabetes tipo 2 em pacientes na faixa etária de 10 a 17 anos. Com a decisão, o fármaco torna-se o primeiro da classe dos agonistas duplos (GIP/GLP-1) liberado para o público pediátrico no Brasil. Anteriormente, a substância era autorizada apenas para adultos com a doença e para controle de peso em casos específicos.
A nova indicação surge como uma alternativa terapêutica para médicos em situações onde tratamentos convencionais não apresentam resultados satisfatórios no controle da glicemia. O medicamento atua em hormônios que regulam a insulina e o apetite, auxiliando na redução dos níveis de açúcar no sangue. A autorização é considerada estratégica pelo setor de saúde, já que o Brasil registra hoje cerca de 213 mil adolescentes com diabetes tipo 2 e outros 1,4 milhão em estado de pré-diabetes.
A aprovação do órgão regulador brasileiro teve como base um estudo clínico internacional de fase 3, cujos resultados foram publicados na prestigiada revista científica Lancet. Os testes demonstraram eficácia no controle glicêmico de crianças e adolescentes, apresentando um perfil de segurança consistente. Os efeitos colaterais relatados foram majoritariamente gastrointestinais, como náuseas e vômitos de intensidade leve a moderada, ocorrendo principalmente nas semanas iniciais de uso.
Apesar da liberação, a Anvisa reforça que o tratamento com a tirzepatida em menores de idade deve ser rigorosamente individualizado e acompanhado por especialistas. Como o público-alvo está em fase crítica de desenvolvimento físico e hormonal, o monitoramento médico contínuo é indispensável para ajustar dosagens e avaliar a resposta do organismo. A medida representa um avanço no manejo de uma doença que tem crescido entre jovens devido a fatores como sedentarismo e mudanças nos hábitos alimentares.


























Comentários: